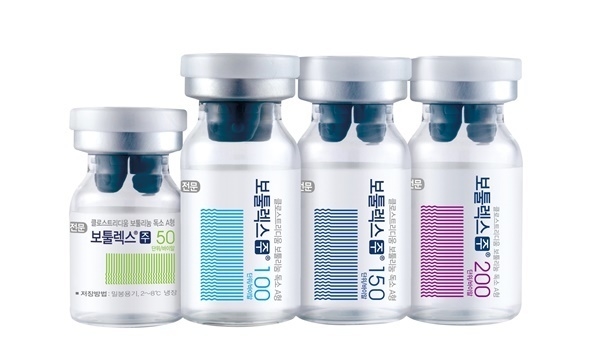
[딜사이트 민승기 기자] 휴젤의 보툴리눔 톡신 제제 보툴렉스가 보건당국으로부터 허가취소 처분을 받았음에도 GS그룹 컨소시엄(APHRODITE ACQUISITION HOLDINGS LLC)과의 인수합병 계획은 차질없이 진행되고 있는 모습이다.
20일 제약·바이오 업계에 따르면 산업통상자원부에서 진행한 국가핵심기술 보유 대상기관(휴젤)의 해외 인수합병 승인이 결정됐다. 휴젤이 보유한 보툴리눔 톡신 제제 생산기술은 국가핵심기술에 해당된다. 따라서 국가핵심기술을 수출하거나 외국인이 해당 기술을 보유한 기업을 인수합병 할 경우 반드시 정부 허가를 받아야 한다. 산자부는 '산업기술의 유출 방지 및 보호에 관한 법률' 등의 규정에 따라 휴젤 인수합병에 대한 심사를 진행한 끝에 최종 승인 결정을 내렸다.
한때 휴젤의 허가취소 논란으로 GS그룹 컨소시엄이 '인수합병을 취소할 수 있다'는 소문이 돌기도 했지만 정부의 이번 인수합병 승인 결정으로 불안감은 모두 해소됐다는 평가다.
GS컨소시엄 역시 허가취소 처분 사유가 안전성과 직결되는 품질 문제가 아니라 유통 관행에 대한 해석 문제일 뿐이고 글로벌 시장 진출에 대한 성공 가능성은 여전히 존재한다고 판단한 것으로 보인다.
애당초 GS그룹 컨소시엄이 무려 1조7000억원을 들여 국내 보툴리눔 톡신 1위 업체인 휴젤을 인수하기로 결정한 이유는 국내 뿐만 아니라 선진 글로벌 시장 진출에 대한 기대감이 반영됐기 때문이다. 이들은 품질 문제가 아니라면 이미 진출해 있는 중국에서의 제품 허가가 유지될 수 있고 미국, 유럽 등에서의 허가를 획득하는데도 문제가 없다고 판단한 것으로 보인다.
투자업계 관계자는 "매출과 직결되는 허가취소 문제였기 때문에 GS그룹 컨소시엄이 계약을 취소할 가능성도 충분히 존재했다"면서 "그러나 산자부의 인수합병 승인 결정까지 별다른 행동을 보이지 않은 것은 충분히 감당할 수 있는 리스크로 판단한 것 아니겠느냐"라고 말했다.
휴젤 보툴렉스 300단위의 허가가 행정처분 대상에서 제외된 것도 긍정적인 신호로 받아들였을 가능성도 있다. 약사법상 동일한 성분의 제품 허가가 유지되고 있으면 별다른 임상시험을 거치지 않고 품목허가를 1년 뒤 재신청 할 수 있다. 보툴리눔 톡신 300단위는 피부미용 목적보다 뇌졸중 등 치료에 사용되는 용량이다.
제약업계 관계자는 "유통 관련 이슈이기 때문에 본안 소송에서도 충분히 붙어볼 만 한 데다가 300단위의 허가가 살아있어 패소 등 최악의 시나리오로 흘러가더라도 빠른 시일 내 시장에 재진입할 수 있자"고 설명했다. 그는 "모든 단위의 제품 허가가 취소되면 처음부터 다시 임상을 시작해야 한다"며 "이 경우 추가적인 임상비용 지출 뿐만 아니라 시장 재진입까지 시간이 너무 오래 걸릴 수 있다"고 덧붙였다.
한편 지난 8월 24일 휴젤 최대주주인 Leguh Issuer Designated Activity Company(이하 LIDAC)는 GS그룹 컨소시엄(APHRODITE ACQUISITION HOLDINGS LLC)과 휴젤 보유주식 535만5651주(총 발행주식의 42.895%) 및 전환사채를 양도한다는 내용의 '최대주주 변경을 수반하는 주식양수도계약(SPA)'을 체결했다.
APHRODITE ACQUISITION HOLDINGS LLC는 GS그룹과 국내 사모펀드 IMM인베스트먼트가 공동 출자한 특수목적법인(SPC)으로 아시아 헬스케어 전문투자펀드 CBC그룹, 중동 국부펀드 무바달라(Mubadala)가 재무적투자자(FI)로 참여했다. 해당 컨소시엄의 최대주주는 CBC그룹이다.
ⓒ새로운 눈으로 시장을 바라봅니다. 딜사이트 무단전재 배포금지

 Home
Home