

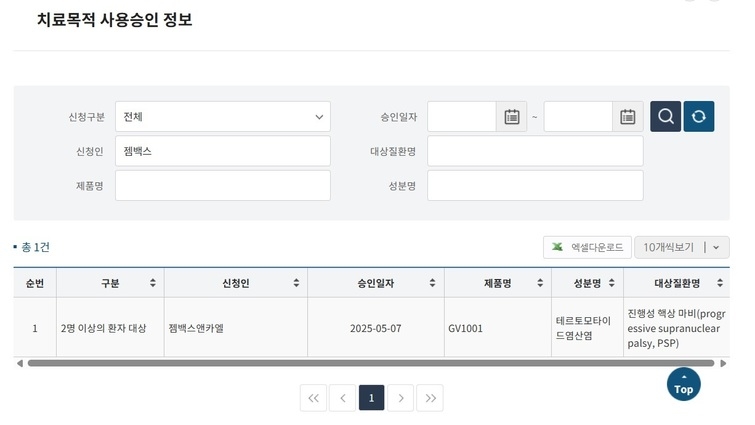
[딜사이트 최광석 기자] 젬백스앤카엘(젬백스)이 현재 개발 중인 진행성핵상마비(PSP) 치료제 'GV1001'의 동정적 사용승인 프로그램(EAP, 치료목적 사용승인)에 대해 긍정적인 입장을 내놨다. 치료제가 없어 신약에 기대를 거는 환자들에게 마지막 희망이 될 수 있다는 인도적 차원의 결단이다. EAP 검토가 가능해진 이유는 이달 초 회사의 PSP 치료제가 미국 식품의약국(FDA)으로부터 패스트트랙(Fast Track) 지정을 받은 덕분이다.
젬백스 관계자는 20일 본지와 통화에서 "중증 환자에게 인도적 차원으로 진행되는 EAP에 적극적으로 동참할 의사가 있다"며 "치료제가 없는 환자에게 치료 기회를 줄 수 있는 부분인 만큼 더 많은 환자들이 혜택을 받을 수 있도록 노력하겠다"고 밝혔다.
EAP는 생명이 위태로울 수 있는 중대한 상황이나 현존하는 치료 방법이 없는 질환에 대해 원칙적으로 임상시험용으로만 사용할 수 있는 의약품을 품목허가 전 치료목적으로 사용할 수 있도록 허용하는 제도다. 국내에는 EAP와 유사한 치료목적 사용승인 제도가 있다. 중대한 질환을 앓고 있는 환자에게 의약품 투여의 위험보다 이익이 크다고 의료진이 판단할 때 활용할 수 있다.
실제 다른 질환에서도 EAP가 활발하게 활용됐다. 노바티스 만성골수성백혈병 치료제 '글리벡'과 아스트라제네카 비소세포폐암 치료제 '이레사', '타그리소' 등 블록버스터 의약품들도 과거 EAP를 통해 환자들에게 공급됐다.
GV1001의 치료목적 사용이 가능해진 배경은 이달 7일 미국 FDA로부터 패스트트랙 지정을 받았기 때문이다. 패스트트랙은 심각한 질환을 치료하고 미충족 의료 수요를 해결할 수 있는 약물의 개발을 촉진하기 위한 제도다.
더불어 패스트트랙 지정으로 ▲FDA와의 긴밀한 소통을 통한 임상 설계 및 의약품 승인 지원에 필요한 적절한 데이터 수집 보장 ▲심사 기간을 단축할 수 있는 롤링 리뷰 ▲가속승인 및 우선심사 신청 등의 혜택을 누릴 수 있다.
앞서 회사는 이달 2일 FDA로부터 희귀의약품 지정(ODD)도 받았다. 희귀의약품으로 지정되면 FDA로부터 ▲임상비용 최대 25% 세액 공제 ▲신약 허가 신청 수수료 면제 ▲시판 후 7년간 시장 독점권 부여 등의 혜택을 받는다.
시장에서는 GV1001의 치료목적 사용이 이뤄질 경우 젬백스의 기대효과도 점치고 있다. 실제 본 임상과는 별개로 효능을 조기에 확인할 수 있는 기회가 될 것으로 보고 있다. 더불어 다른 질환으로의 적응증 확대 가능성을 엿보는 계기가 될 수 있다고 전망하고 있다.
시장 한 관계자는 "FDA 패스트트랙 및 희귀의약품 지정은 신약으로서 어느 정도 가능성을 인정받은 것"이라며 "앞으로 임상이 속도감 있게 추진될 것으로 보이며 상용화에 대한 기대감도 커질 전망"이라고 말했다.
한편 PSP는 균형장애, 안구운동장애, 언어 및 인지기능 저하 등을 유발하는 비정형 파킨슨증후군으로 파킨슨병과 유사한 증상을 보이지만 진행 속도가 훨씬 빠르다. 현재까지 근본적인 치료제가 없어 새로운 치료 옵션에 대한 미충족 의료 수요가 높은 질환으로 알려졌다.
ⓒ새로운 눈으로 시장을 바라봅니다. 딜사이트 무단전재 배포금지

 Home
Home

















